Competencia Económica y Consumo
12 de febrero de 2020
Confusión y medicamentos: marcas farmacéuticas
Por: Lina María Díaz Vera - LLM, Investigadora
La trágica muerte de dos menores de edad por el suministro equivocado del opioide Tramadol en lugar del purgante Albendazol destaca por qué es tan importante la regulación de la imagen comercial (trade dress), las marcas y envases de los medicamentos que se suministran a los pacientes, de forma que se suministre la información necesaria para reducir errores humanos. Según la Organización Mundial de la Salud, en el mundo 4 de cada 10 pacientes sufren de daños en atención de salud sanitaria primaria o ambulatoria, dentro de los errores más dañitos están asociados a diagnóstico, prescripción y uso de medicamentos**.
Las marcas suministran a los consumidores información acerca de la calidad, origen empresarial y precio de un producto. Por ello, cuando se evalúa si un signo es susceptible de registro como marca se analizan varios aspectos: que sea perceptible por cualquiera de los sentidos, que tenga representación gráfica, que tenga distintividad. Para el caso del registro de marcas de medicamentos hay otros aspectos por considerar. En primer lugar, el Tribunal Andino de Justicia ha resaltado que cuando se trata de marcas farmacéuticas se debe ser especial cuidadoso para que el signo no genere confusión entre los consumidores medios, ya que ello puede tener gravísimas consecuencias.
El Tribunal Andino ha señalado lo siguiente:
“En principio, los productos farmacéuticos y los otros PRODUCTOS de la clase 5 pueden tener canales de comercialización diferentes y expendedores calificados, en el uso y la manipulación de los mismos puede generarse confusión en el público consumidor, tal como sería el caso del almacenamiento y el posterior consumo de dichos productos en el hogar o en almacenajes privados de cualquier clase. Lo anterior, porque estos están al acceso del consumidor ordinario, que bien puede confundirse y aplicar un producto destinado para otro fin; es muy posible que el consumidor que por alguna razón tiene a su alcance dichos productos pueda caer en un error, lo que podría ser fatal para su salud o para la salud de los animales o plantas a los que se le aplica”.[1] (Se resalta)
De otra parte, cuando se trata del registro de marcas farmacéuticas, cobran especial relevancia los apartados e y f del Artículo 135 de la Decisión 486 de 2000. Estas normas prohíben que se registre como marca los signos que consistan exclusivamente en indicaciones o datos acerca de las características o información de los productos, así como el nombre genérico o técnico del producto de que se trate. Los medicamentos están compuestos por activos químicos que tienen una Denominación Común Internacional (DCI) –International Nonproprietary Names INNs-, la cual es asignada por un Grupo de Expertos de la Organización Mundial de la Salud (OMS). Así, no puede registrarse como marca una DCI[2].
El objetivo de las DCI es proporcionar a los profesionales en salud un nombre único y universal para identificar cada sustancia farmacéutica, de esta forma, al contar con una nomenclatura internacional se logra una identificación clara para la prescripción, venta y dispensación de medicamentos a los pacientes y para la comunicación e intercambio de información entre científicos en todo el mundo[3]. Por esto, la OMS solicita a los países que tomen las medidas necesarias para evitar que se registren como marcas las DCI cada vez que se realiza una adición o modificación a las mismas, pues las marcas pueden expirar o cambiar, pero mientras se emplee la sustancia, debe permanecer la DCI[4]. Además, la DCI toma medidas para evitar que expresiones que se encuentren registradas como marcas se incluyan dentro de las DCI[5].
“Pertenezco a todos pero no soy propiedad de nadie.
Me llaman de la misma manera en la mayoría de los idiomas, y significo lo mismo en todo el mundo.
Me parezco a mis semejantes, pero soy distinto de los 8.500 que me precedieron.
Soy una denominación común internacional (DCI), un nombre genérico exclusivo asignado a casi todos los principios activos utilizados en los medicamentos de todo el mundo.”[6]
Ahora bien, otro elemento que ayuda a los consumidores a diferenciar un producto de otro es la forma del producto, su envase o envoltura, lo que se conoce como el trade dress y que en virtud del artículo 134(f) de la Decisión 486 de 2000 también puede registrarse como marca. Por supuesto, para el caso de los medicamentos existe una amplia regulación en cuanto a la información que se debe suministrar en la envoltura y etiquetas de estos productos. El Decreto 677 de 1995 señala la información que deben contener las etiquetas, rótulos y empaques de los medicamentos, los cuales deben ser aprobados por el INVIMA antes de ser comercializados. Allí se indica que en el empaque se debe señalar el nombre del producto, marca registrada y la denominación genérica o DCI de la sustancia de que se trate.
A fin de aumentar la seguridad en el suministro de medicamentos y evitar confusiones con desenlaces fatales, en otros países se ha impulsado una regulación adicional para que los envases de los medicamentos sean aún más claros para médicos, distribuidores y consumidores finales. Debido a que un mismo medicamento puede ser distribuido tanto en una versión original como en una versión genérica es posible que el mismo medicamento se comercialice con diferentes presentaciones. Por ejemplo, el Omeprazol en España tiene más de 40 presentaciones genéricas y más de 20 no genéricas, de forma que un paciente que requiere este medicamento podría recibir más de 60 envases diferentes[7].
Por ello, en España se discute un proyecto legislativo para que los “fármacos que sean iguales, parezcan iguales y no confundan a los consumidores”, lo que se conoce como isoapariencia[8]. La propuesta consiste en que en una de las caras con mayor superficie del envase se incluya el equivalente a la DCI, la dosis del medicamento y el número de dosis sobre fondo blanco[9]. Con esto no solo se espera reducir el riesgo de confusión de los medicamentos sino que los pacientes sean más persistentes con los tratamientos.

Imagen tomada del Blog Sano y Salvo[10]
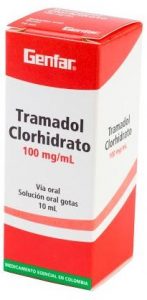
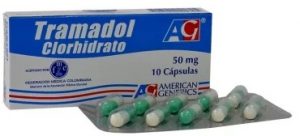
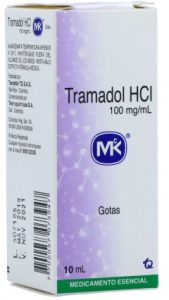
Ahora bien, si se analiza lo que sucede en Colombia, cómo se comercializan los medicamentos genéricos, es posible notar un patrón, cada laboratorio cuenta con un trade dress diferente y característico que muchas veces se encuentra registrado como marca mixta, lo único que a primera vista diferencia un medicamento de otro dentro de los productos de un mismo laboratorio es el nombre de la sustancia activa, como se puede ver en seguida:
| Genfar | MK | American Generics |

Certificado: 608843 |

Certificado: 368687 |

Certificado: 415927 Caducada |

Certificado: 608803 |

Certificado de registro: 469465 |
|
|
No registrada |
No registrada |
No registrada |
Elaborado con fundamento en información del Sipi.
Como permiten observar las anteriores imágenes, es importante que las personas involucradas con el suministro de medicamentos, especialmente cuando se trata de genéricos, se fijen especialmente en el nombre de la sustancia o DCI que contiene el empaque y no tanto en el trade dress del mismo, además, por supuesto, de cumplir rigurosamente con otras disposiciones atenientes con el almacenamiento y dispensación de medicamentos, especialmente los que están sujetos a control y sólo se pueden suministrar con fórmula médica. Por ejemplo, en el suministro de medicamentos es especialmente importante que lea en voz alta el nombre del fármaco que se entrega al paciente y se corrobore con la fórmula médica para que también el consumidor verifique el producto que recibe.
En conclusión, en la legislación actual hay mecanismos para evitar que se confunda un medicamento con otro y que esto tenga consecuencias nefastas en la salud de personas, animales y plantas, para que los envases de medicamentos cuenten con información suficiente para que médicos, dispensarios y pacientes puedan decidir sobre la conveniencia de tomar un medicamento o no. Sin embargo, dados los hechos recientes es importante evaluar si esta regulación es suficiente o si son necesarios más mecanismos para eliminar el riesgo de confusión.
** Organización Mundial de la Salud. Alianza Mundial para la Seguridad del Paciente. La investigación en Seguridad del Paciente.
[1] Proceso 35-IP-2011. Marca: “KILOL”, publicado en la Gaceta Oficial Nº 1985, de 28 de septiembre de 2011.
[2] Las DCI se crearon en 1950 con la Resolución WHA3.11 de la Asamblea Mundial de Salud.
[3] World Health Organization. Guidance on the use of International Nonproprietary Names (INNs) for Pharmaceutical Substances. 2017. Pág. 5.
[4]Grupo de Expertos en Denominación Común Internacional. Organización Mundial de la Salud. La importancia del Nombre. Disponible en: https://www.who.int/features/2013/international-nonproprietary-name/es/ Consultado el 27/01/2020.
[5] World Health Organization. Guidance on the use of International Nonproprietary Names (INNs) for Pharmaceutical Substances. 2017. Pág. 6
[6] Grupo de Expertos en Denominación Común Internacional. Organización Mundial de la Salud. La importancia del Nombre. Disponible en: https://www.who.int/features/2013/international-nonproprietary-name/es/ Consultado el 27/01/2020.
[7] Lapuente, F., & Rodríguez, M. (2011). Isoapariencia. una necesidad imperiosa en la prescripción por denominación oficial española. Atención Primaria, 43(12), 625-6. doi:10.1016/j.aprim.2011.11.001
[8] Campillo, E. La isoapariencia, el ‘antídoto’ deseado aunque complejo contra los errores en la medicación. En El Global. 4 de mayo de 2018. Consultado el 27/01/2020. Disponible en: https://elglobal.es/farmacia/la-isoapariencia-el-antidoto-deseado-aunque-complejo-contra-los-errores-en-la-medicacion-IE1521813/
[9] Lapuente, F., & Rodríguez, M. (2011). Isoapariencia. una necesidad imperiosa en la prescripción por denominación oficial española. Atención Primaria, 43(12), 625-6. doi:10.1016/j.aprim.2011.11.001
[10] Sano y Salvo. En los medicamentos, las apariencias importan. Publicación en AMF del artículo “Isoapariencia: si son iguales que parezcan iguales” y el caso de la confusión de sueros en un hospital de Parla. Disponible en: http://sano-y-salvo.blogspot.com/2016/10/en-los-medicamentos-las-apariencias.html
Consultado el 27/01/2020.